Pourquoi le ciel est-il rouge le matin et le soir, et bleu en milieu de journée ? L’explication se lit, non pas dans le marc de café, mais dans de l’eau additionnée d’un peu de lait écrémé. Voici une expérience facile à réaliser et au contenu pédagogique très riche..
Fiche d’accompagnement de l’expérience:
 Matériel
Matériel- une cuve transparente ;
- une lampe torche ou une lanterne de laboratoire ;
- du lait écrémé
- nitrate d’argent
- thiosulfate de sodium
- acide chlorhydrique dilué.
 Montage et réalisation
Montage et réalisationVerser quelques gouttes de solution de nitrate d’argent ou bien ajouter dans 100 ml d’eau 2 g de thiosulfate de sodium et 100 ml d’acide chlorhydrique dilué dans une cuve transparente remplie d’eau et bien mélanger.
Nous avons choisi ici de verser quelques gouttes de lait écrémé dans une cuve transparente remplie d’eau et bien mélanger.
Eclairer le dispositif avec le faisceau d’une lampe torche.
Vue de côté, la solution est d’un blanc bleuté. Si l’on regarde la lampe à travers la solution, celle-ci paraît rouge. Si l’on augmente la concentration en lait écrémé, la face de la cuve opposée à la lampe paraît rouge vue de côté, et la face de la cuve proche de la lampe devient bleue.
 Explications
ExplicationsLa lumière de la lampe de poche contient presque toutes les longueurs d’onde visibles. La diffusion ne peut pas se manifester dans une substance homogène (l’eau par exemple) car la diffusion Rayleigh se produit avec des particules isolées de dimensions faibles par rapport à la longueur d’onde de la lumière.
C’est la raison pour laquelle on ajoute ici à l’eau d’autres substances (par exemple celles qui sont proposées pour l’expérience). Les centres de diffusion que constituent les ions Ag+ et NO3- en solution ont des dimensions nettement inférieures à la longueur d’onde de la lumière utilisée. Ces ions sont le siège des phénomènes décrits ci-dessous.
Le champ électrique du rayonnement électromagnétique agit sur la répartition des électrons de la molécule (appellation générale, ici il s’agit de l’ion Ag+). Il entraîne l’apparition d’un moment dipolaire induit 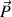 à l’intérieur de la molécule. Le champ électrique induit
à l’intérieur de la molécule. Le champ électrique induit 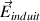 compense le champ électrique extérieur
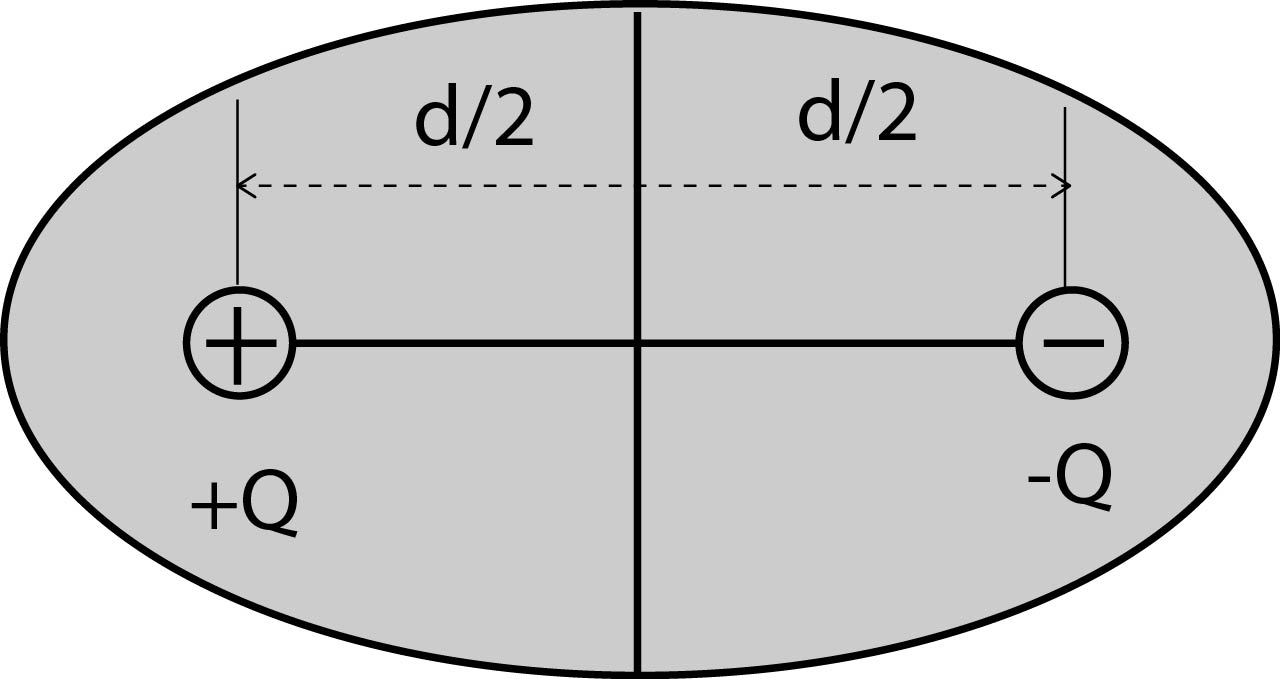
compense le champ électrique extérieur 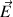 dans la région située entre les charges +Q et –Q du dipôle
dans la région située entre les charges +Q et –Q du dipôle
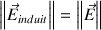
La valeur du champ induit entre les charges +Q et –Q est :
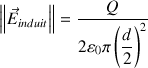
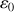 : constante diélectrique du vide ;
: constante diélectrique du vide ;
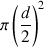 : surface approximative de la section de la molécule ; d : distance moyenne entre les barycentres des charges négatives et positives).
: surface approximative de la section de la molécule ; d : distance moyenne entre les barycentres des charges négatives et positives).
On a alors pour le moment dipolaire :
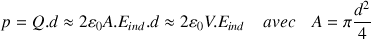
(où V = A.d est le volume approximatif de la molécule).
Comme la valeur E du champ électrique extérieur dépend de la pulsation 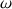 de la lumière incidente, la valeur
de la lumière incidente, la valeur 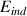 du champ électrique induit en dépend aussi.
du champ électrique induit en dépend aussi.
Selon Heinrich Hertz (1857-1894), le dipôle rayonne alors la puissance P telle que :
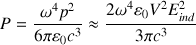
(c : vitesse de la lumière dans le vide).
Cette puissance est prélevée à l’onde incidente. L’onde incidente a pour intensité
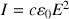 .
.
Il en résulte pour la section efficace de diffusion 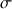 l’expression suivante :
l’expression suivante :
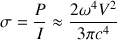
Comme la section efficace de diffusion s est proportionnelle à 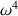 elle est environ 16 fois plus grande pour la lumière bleue (λ ≈ 400 nm) que pour la lumière rouge (λ ≈ 800 nm). La lumière bleue subit une diffusion beaucoup plus importante que la lumière rouge. Ce mécanisme de diffusion est appelé diffusion Rayleigh.
elle est environ 16 fois plus grande pour la lumière bleue (λ ≈ 400 nm) que pour la lumière rouge (λ ≈ 800 nm). La lumière bleue subit une diffusion beaucoup plus importante que la lumière rouge. Ce mécanisme de diffusion est appelé diffusion Rayleigh.
Lorsqu’on acidifie une solution de thiosulfate de sodium, il se produit la réaction suivante :
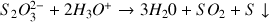 La lumière subit alors une diffusion Rayleigh sur les particules de soufre formées qui, tout comme les ions nitrate, ont des dimensions très inférieures à la longueur d’onde de la lumière visible.
La lumière subit alors une diffusion Rayleigh sur les particules de soufre formées qui, tout comme les ions nitrate, ont des dimensions très inférieures à la longueur d’onde de la lumière visible.
Le lait contient des particules de matière grasse dispersées dans une solution aqueuse. Ces particules sont à peine plus grandes que la longueur d’onde de la lumière visible. La diffusion de la lumière par ces particules s’appelle « diffusion de Mie » – elle doit son nom à Gustav Mie (1868-1957). La section efficace de diffusion dépend ici encore de la fréquence de la lumière incidente, mais de façon moins marquée que pour la diffusion Rayleigh (il ne s’agit plus d’une loi en 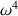 ). C’est la raison pour laquelle on observe avec le lait des résultats analogues aux résultats obtenus avec les substances qui permettent de montrer la diffusion Rayleigh.
). C’est la raison pour laquelle on observe avec le lait des résultats analogues aux résultats obtenus avec les substances qui permettent de montrer la diffusion Rayleigh.
 Remarques
Remarques
Contrairement à un liquide pur, l’air ne présente pas une structure régulière : sa densité subit des discontinuités importantes sur de faibles distances. La lumière solaire subit donc une diffusion sur les molécules de l’air selon le mécanisme de la diffusion Rayleigh (les dimensions des molécules de l’air sont nettement inférieures à la longueur d’onde de la lumière visible).
La distance caractéristique d’absorption l d’une lumière de longueur d’onde l est donné par la formule suivante :
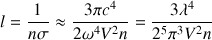
n : densité volumique des particules ;
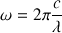 : pulsation de l’onde
: pulsation de l’onde
On peut calculer l’ordre de grandeur du volume moléculaire V à partir de la masse volumique 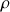 de l’air liquide (pratiquement égale à celle de l’eau), car l’état liquide est un état condensé dans lequel les molécules sont jointives :
de l’air liquide (pratiquement égale à celle de l’eau), car l’état liquide est un état condensé dans lequel les molécules sont jointives :
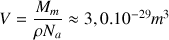
( 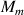 = 18 g.mol-1 :
= 18 g.mol-1 : 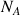 masse molaire de l’eau;
masse molaire de l’eau; 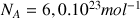 : constante d’Avogadro).
: constante d’Avogadro).
On calcule n, densité volumique des molécules dans l’air, à l’aide de la formule suivante :
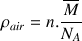
( 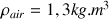 : masse volumique de l’air ;
: masse volumique de l’air ; 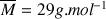 1 : masse molaire moyenne de l’air.
1 : masse molaire moyenne de l’air.
On obtient 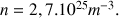 Avec la valeur estimée pour V et celle qui a été calculée pour n on obtient pour la distance caractéristique d’absorption l dans l’air d’une lumière de longueur d’onde
Avec la valeur estimée pour V et celle qui a été calculée pour n on obtient pour la distance caractéristique d’absorption l dans l’air d’une lumière de longueur d’onde 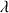
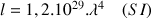
Pour le violet (400 nm) on calcule une distance caractéristique d’absorption de 3,2 km, pour le rouge (800 nm) de 51 km et pour le jaune (600 nm) de 16 km. Lorsque le soleil est haut sur l’horizon, seuls le violet et le bleu sont diffusés. Au lever et au coucher du soleil, quand le parcours de la lumière à travers l’atmosphère (d’épaisseur 8 km) dépasse 300 km, seul le rouge parvient encore (atténué) jusqu’à l’œil.
John William Strutt, Lord Rayleigh (1842-1919), prix Nobel en 1904, a compris en 1899 que la lumière solaire est diffusée surtout par les molécules de l’air et pas seulement par les impuretés contenues dans l’air. Cette interprétation avait été donnée en 1868 par John Tyndall (1820-1893) qui avait étudié le « smog » londonien (selon [Glass 1997, p. 87], Tyndall avait proposé de réaliser l’expérience que nous venons de décrire en ajoutant à l’eau quelques gouttes d’eau de Cologne pour obtenir des particules diffusantes). Rayleigh avait énoncé dès 1871 que l’intensité de la lumière diffusée est inversement proportionnelle à la puissance quatrième de la longueur d’onde.
C’est parce que la lumière bleue est plus diffusée que la lumière rouge que les feux de brouillard arrière des voitures sont rouges (et les phares jaunes).

