L’eau pure et très peu conductrice : un circuit électrique dont deux conducteurs plongent dans un récipient d’eau ne permet pas le passage d’un courant et l’éclairage d’une lampe. En revanche, si on dissout du sel dans l’eau, la lampe s’éclaire rapidement.
Fiche d’accompagnement de l’expérience:

 Matériel
Matériel- une pile plate (4,5 V) ;
- une ampoule de lampe de poche (2 W) ;
- des fils électriques ou du fil de cuivre isolé ;
- un verre ou un gobelet ;
- du gros sel.
 Montage et réalisation
Montage et réalisationRemplir un verre avec de l’eau du robinet. Prendre trois morceaux de fil électrique d’environ 20 cm et les dénuder aux extrémités.
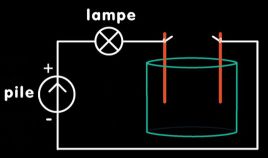
Relier un bout du premier fil à l’un des pôles de la pile et introduire l’autre bout dans l’eau. Prendre le deuxième fil, le relier par une extrémité à la lampe et laisser l’autre extrémité dans l’eau. Relier la lampe à la pile par le troisième fil (voir figure) : la lampe ne brille pas. Verser du gros sel dans l’eau : la lampe se met à briller. Elle brille d’autant plus qu’on a dissous davantage de sel dans l’eau.
 Explications
ExplicationsCe sont les ions qui permettent au courant de traverser certaines solutions aqueuses.
La conductivité dépend notamment des concentrations en anions et en cations. L’eau du robinet contient en général trop peu de porteurs de charges : sa conductivité et donc l’intensité du courant sont alors trop faibles pour que la lampe s’allume.
L’ajout de gros sel augmente le nombre des porteurs de charges car la dissolution du chlorure de sodium donne des ions sodium Na+ et des ions chlorure Cl-. Sous l’effet du champ électrique les ions se déplacent vers les électrodes. A l’anode, les ions chlorure sont oxydés en dichlore dont une partie reste en solution dans l’eau tandis qu’une autre partie se dégage sous forme de gaz. A la cathode, les molécules d’eau sont réduites en dihydrogène qui s’échappe.
Plus la quantité de sel dissous augmente, plus la concentration des porteurs de charges augmente et plus la conductivité de la solution augmente. La résistivité (inverse de la conductivité) de la solution est de 94 Ω.m pour une concentration de 1 mol.m-3 et de 9,8 Ω.m pour une concentration de 10 mol.m-3.
La lampe brille d’autant plus que la quantité de sel dissoute augmente car la conductivité est pratiquement proportionnelle à la concentration. Cette relation de proportionnalité entre la conductivité et la concentration en sel dissous n’est valable que jusqu’à une concentration maximale égale à 70% de la solubilité du sel dans l’eau. Au-delà, la conductivité tend vers une valeur limite.
 Références
RéférencesUniversité en Ligne : le courant électrique

